"Enlace químico"
Es el proceso físico responsable de las interacciones atractivas entre átomos y moléculas. y que confieren estabilidad a los compuestos químico diatomicos y poliatomicos.
La explicación de tales fuerzas atractivas es un área compleja que esta descrita por las leyes de la electrodinámica cuántica.
Sin embargo, en la practica, los químicos suelen apoyarse en la mecánica cuántica en descripciones cualitativas que son menos rigurosas, pero mas sencillas en su propia descripción del enlace químico.
ENLACE IÒNICO.
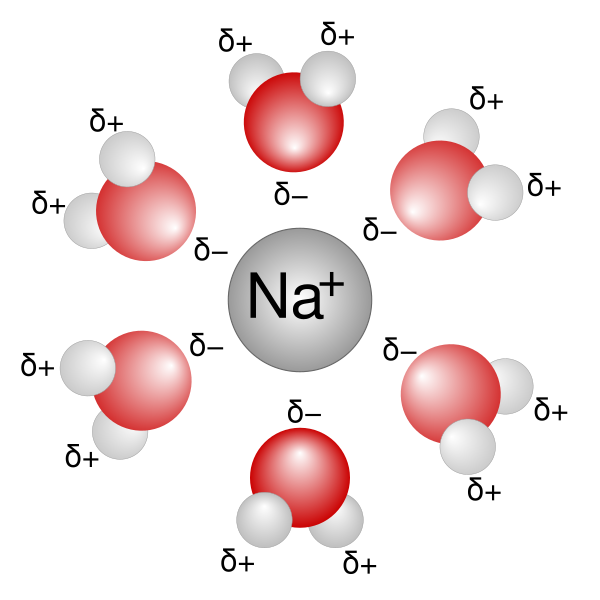
El enlace iònico consiste en la atracción electrostática entre átomos con cargas electricas de signo contrario.Este tipo de enlace se establece entre átomos de elementos poco electronegativos con los de elementos muy electronegativos.
Es necesario que uno de los elementos pueda ganar electrones y el otro perderlo, y como se ha dicho anteriormente este tipo de enlaces suele producir entre un no metal y un metal.
ENLACE COVALENTE.
Los elementos tienen la tendencia a conseguir configuracion electrónica de gas noble (8 electrones en la ultima capa).Elementos situados a la derecha de la tabla periódica(no metales)consiguen dicha configuracion por captura de electrones;elementos situados a la izquierda y en el centro de la tabla (metales),la consiguen por perdida de electrones.